En un momento de cambio como el actual, los e-CRD deben ocupar un lugar destacado en cualquier tipología de estudio de Investigación Clínica, ya sean observacionales o ensayos clínicos. Un buen e-CRD debe poder dar cobertura a las necesidades de cada uno de los participantes en el estudio convirtiéndose, por tanto, en una plataforma de gestión que permita una reducción global de costes, facilite el trabajo de reclutamiento a los Investigadores y, por supuesto, ofrezca una mejora en la calidad de los datos con una significativa reducción de tiempo desde el cierre de BBDD hasta la obtención de resultados.

Hace años que los e-CRD se han incorporado al mundo de la investigación clínica, y se ha escrito mucho acerca de los beneficios que deberían ofrecer a los estudios, pero lo cierto es que a fecha actual continúa siendo un área en la que no se ha avanzado lo suficiente. Actualmente la tecnología nos ofrece grandes posibilidades para conseguir que los e-CRD pasen de ser simples formularios electrónicos, para la entrada de datos a auténticas herramientas de gestión, que faciliten el seguimiento de los estudios atendiendo a las diferentes necesidades de las partes implicadas (Promotor, Investigadores, CRO, Coordinadores, …).
Es indudable que en estos últimos años, y acelerado por la crisis y los recortes que en el sector estamos sufriendo, el modelo de negocio ha variado y desde la industria cada vez se necesitan mejores soluciones que permitan reducir los costes en el desarrollo de proyectos de investigación clínica, facilitando la labor de investigadores y asegurando la calidad de los datos generados en los estudios que se llevan a cabo.
La solución tiene que venir de un nuevo enfoque en el desarrollo de los e-CRD, consiguiendo que éstos evolucionen hacia verdaderas plataformas de gestión que integren, en un entorno amigable y de alta usabilidad, todas las funcionalidades necesarias para incentivar su uso y ofreciendo un valor diferencial respecto al desarrollo de los estudios, con el tradicional CRD en papel o el simple formulario electrónico, que no ofrece más que la introducción de datos a través de la web.
Desde las CROs debemos ser capaces de ofrecer soluciones específicas a cada uno de los participantes en los proyectos que lideramos y, por tanto, actuar como consultores ofreciendo soluciones innovadoras que permitan optimizar los procesos y ofreciendo herramientas que faciliten e incentiven las etapas de desarrollo de los estudios (regulatorio, reclutamiento, explotación, …)
En la compañía que represento creemos firmemente en los beneficios que la tecnología puede y tiene que aportar al sector y contamos con un departamento propio de TI, que nos permite el desarrollo a medida en cada uno de los estudios que abordamos evitando, de esta manera, la estandarización. Cada estudio tiene unas necesidades específicas que deben definirse en la fase inicial con una doble visión clínica y tecnológica, para asegurar una cobertura global y que el e-CRD resultante actúa como driver facilitando el trabajo de los investigadores, a la vez que ofrece la máxima información a coordinadores y promotores del estudio en tiempo real.
El objetivo principal, en el que centramos gran parte del esfuerzo inicial, es conseguir que el e-CRD sea amigable e intuitivo. Se debe alcanzar la máxima sencillez en el módulo de introducción de datos del estudio, pero sin prescindir de los filtros necesarios que garantizarán la calidad de los datos e incorporando sistemas automáticos de auditoría que nos avisen en tiempo real de las inconsistencias detectadas. Con esta filosofía, aplicada desde el origen, se consigue acelerar el cierre de la base de datos y obtener una reducción de costes en tareas de Monitorización.
Hemos dejado atrás el concepto clásico de e-CRD para ofrecer plataformas de gestión donde el formulario de datos es una parte importante pero sobre el que se incorporan, a criterio del promotor, módulos de valor añadido que facilitan el trabajo a la vez que fidelizan a los Investigadores participantes.
En los estudios participan diferentes perfiles profesionales (Promotor, Investigador, Coordinador, CRA,…), y cada uno de ellos tiene unas necesidades específicas que deben quedar cubiertas con la incorporación de módulos adicionales en las nuevas plataformas de gestión:
* Auditoría de Datos: Una de las grandes ventajas que aportan los e-CRD es la posibilidad de realizar auditorías en tiempo real sobre los datos incorporados, pudiendo lanzar alertas a los participantes en el estudio para que puedan ser corregidas incluso antes de la monitorización y, consiguiendo con ello, un gran ahorro en tiempo del estudio y costes de revisión.
* Estadísticas: Permite realizar de forma rápida una consulta de la situación de reclutamiento y seguimiento de los pacientes, así como validar la calidad de los datos según la propia auditoría del sistema.
En función del perfil profesional que acceda al sistema, las estadísticas ofrecerán mayor información agregada y de esta manera el promotor podrá, de forma rápida, conocer el estado de reclutamiento y calidad de los datos a nivel de Investigador, Centro, Área, Comunidad.
* Calendario del Investigador: En base a las fechas de visita el sistema genera alertas automáticas de seguimiento de los pacientes de forma que, tanto investigadores cono promotor, pueden conocer las visitas que deberían haberse realizado y no se han llevado a cabo. Igualmente y para evitar la pérdida de seguimiento de pacientes, pueden programarse con anterioridad y recibir los avisos vía e-CRD, correo electrónico o vía SMS para poder programar las visitas incluso enviando recordatorios al propio paciente.
* Avance de Resultados: Permite obtener una visión preliminar del avance de los datos de las variables principales de forma que incentiva a la continuación del estudio y permite la toma de decisiones en función de los resultados anticipados.
* Repositorio Documental: Un único lugar donde se puede consultar la documentación editada relativa al estudio, así como recibir a través de este módulo las newsletter de evolución del mismo, a la vez que recibe un aviso de nuevos documentos a través de su correo electrónico.
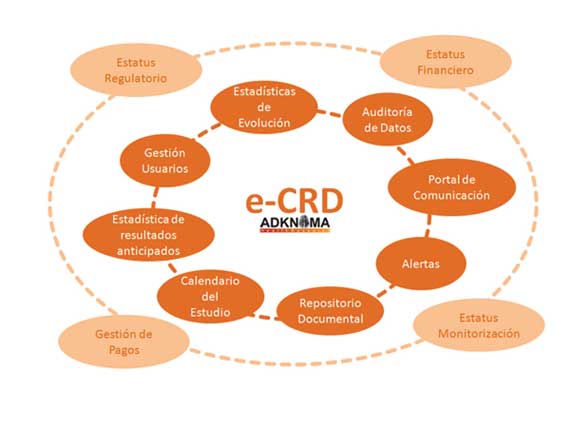
Por supuesto a estas plataformas se las puede enriquecer tanto como el promotor del estudio nos solicite, incorporando la evolución, resultado e informes de monitorización, seguimiento de la fase regulatoria,…
Se ha iniciado un nuevo camino en los proyectos de investigación clínica, y la tecnología nos lo facilita con la introducción de dispositivos como “tablets” que permiten trabajar en cualquier lugar sin problemas de comunicaciones a un coste bajo. Según datos publicados con anterioridad, los estudios que incorporaban el uso del e-CRD como simple formulario electrónico conseguían:
* Reducir el número de queries emitidas.
* Reducir el tiempo medio de resolución en un 35%.
* Iniciar antes la obtención de resultados.
* Reducir globalmente los costes de los proyectos.
Con la introducción de la plataforma de gestión añadimos otras ventajas que con el simple e-CRD no se conseguían:
* Mayor implicación del Investigador en el estudio.
* Mayor prestigio del promotor hacia la sociedad científica.
* Mayor control del estado de reclutamiento.
* Mejor seguimiento del avance de las variables del estudio.
* Reducción en las pérdidas de seguimiento de los pacientes gracias a la introducción del sistema de alertas.
* Mayor satisfacción por parte del promotor del estudio que obtiene información constante de la evolución y calidad de los datos.
* Pensando en las necesidades del Promotor, es posible obtener una visión agregada de todos los estudios que están en marcha y que quedan soportados por la plataforma de Gestión.
En resumen, nuestra visión es que el e-CRD, como simple formulario electrónico de recogida de datos, no aporta valor añadido a la Investigación Clínica. Es la evolución hacia plataformas de gestión desarrolladas a medida para cada estudio, lo que representa el salto definitivo para que la tecnología se consolide de forma definitiva en el desarrollo de cualquier proyecto de investigación clínica, incrementando la eficiencia y reduciendo de forma global los costes.















